Ученые поняли, почему клетки при болезни Альцгеймера "поедают" сами себя
МОСКВА, 2 сен — РИА
новости. Международная группа ученых, в которую вошли сотрудники
Университета ИТМО, вуза — участника Проекта 5-100, выяснила, почему
мутация или отсутствие рецептора TREM2 в иммунных клетках нервной
системы повышает риск развития болезни Альцгеймера. Оказалось, что
иммунные клетки в этом случае перестают получать питание и начинают
"переваривать" самих себя. Свое открытие исследователи описали в журнале
Cell.
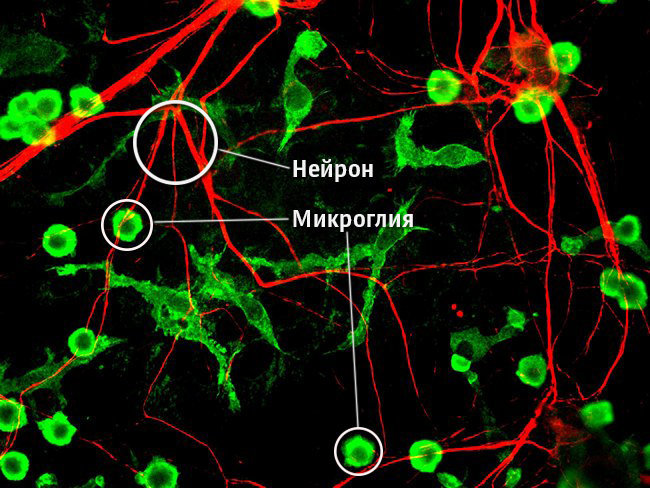
Иммунные клетки нервной системы называются микроглией. Их
главная функция — фагоцитоз, то есть поглощение и уничтожение вредных
чужеродных частиц, в том числе умерших нейронов. Микроглия также
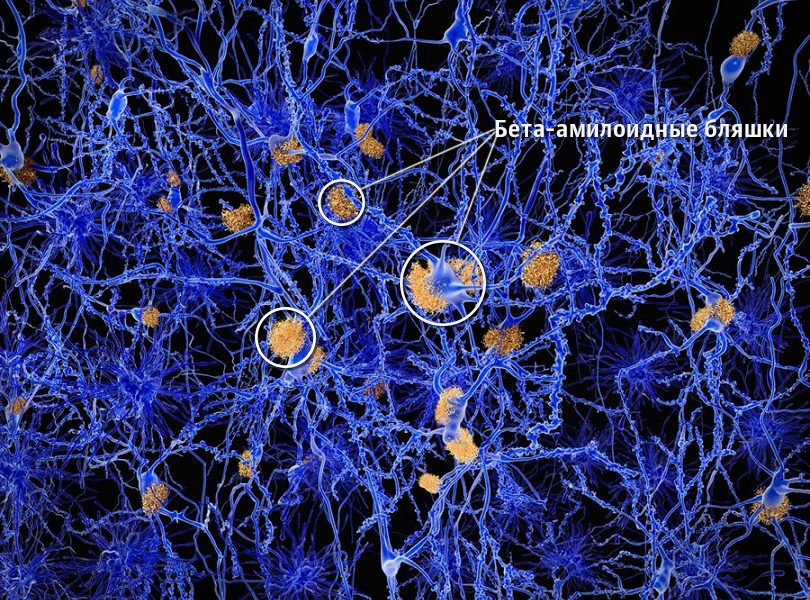
"поедает" бета-амилоиды. Когда эти белки быстро "удаляются" микроглией,
то совершенно безвредны. Однако если этого не происходит, то
бета-амилоиды начинают формировать вокруг нейронов уплотнения — бляшки
из самих себя. В результате нормальная жизнедеятельность нейрона
нарушается, в том числе перестают образовываться синаптические связи
между нервными клетками, а сам нейрон погибает. Все это, наряду с
другими факторами, приводит к болезни Альцгеймера.
На фото показано расположение клеток микроглии и нейронов в мозге человека
Почему
же так происходит? Что случается с микроглией, когда она перестает
выполнять свою важную функцию? Международная группа ученых выяснила, что
одной из причин может быть отсутствие либо мутация рецептора TREM2 у
этих иммунных клеток. В исследовательскую группу вошли сотрудники
Университета ИТМО и Университета Вашингтона в Сент-Луисе.
Работа
по изучению белка TREM2 уже несколько лет ведется в Университете
Вашингтона в Сент-Луисе. Ранее было известно, что рецептор действительно
влияет на иммунный ответ нервной системы, то есть на работу микроглии
по уничтожению отмерших клеток, бета-амилоидов, поврежденного миелина и
других ненужных веществ. Однако не было до конца понятно, как именно это
проявляется. Благодаря эксперименту на мышах ученые поняли, что
отсутствие или мутации в TREM2 вызывают в микроглии аутофагию. Это
значит, что клетки начинают уничтожать самих себя из-за нехватки
питательных веществ. Из-за этого клетки микроглии не могут защищать
нервную систему от вредных веществ, в том числе бета-амилоидных бляшек,
которых с возрастом становится все больше.
На рисунке показаны бета-амилоидные бляшки в мозге человека
Ученые
проводили эксперимент с мышами, у которых не было TREM2 и которые
генетически были предрасположены формировать бета-амилоидные бляшки в
нервной системе. Ученые предположили, что если дать мышам определенную
питательную смесь, то способность их микроглии разрушать бета-амилоиды
восстановится. Так и произошло. Чтобы проверить открытие, ученые в
течение шести месяцев проводили эксперимент уже с двумя группами мышей.
Одним давали смесь, а другим нет, при этом у обеих групп не было TREM2. В
результате мыши, которые получали дополнительное питание, были меньше
подвержены эффектам болезни Альцгеймера.
Химическая формула креатина
Смесь,
которую использовали ученые, — это циклокреатин, а также креатин —
азотосодержащая карбоновая кислота, которая участвует в энергетическом
обмене в мышечных и нервных клетках. Креатин можно использовать в
качестве пищевой добавки для спортсменов с целью повышения выносливости и
роста мышечной массы, однако при этом его прием связывают с вредным
воздействием на сердце, почки и обменные процессы. Поэтому авторы
исследования, опубликованного в Cell, категорически не рекомендуют
применять препараты креатина с целью улучшения здоровья пожилых людей.
Сейчас ученые намерены начать поиск безопасных аналогов креатина, чтобы с
их помощью поддерживать работу микроглии.
Руководитель группы по биоинформатике в лаборатории "Компьютерные технологии" Университета ИТМО Алексей Сергушичев
"TREM2
регулирует так называемый сигнальный путь mTOR, который активирует
нормальный энергетический метаболизм. Когда TREM2 сломан в макрофагах и
микроглии, этот путь подавляется, вызывая метаболические нарушения. Как
именно это происходит, еще не понятно. Креатин и циклокреатин могут
попадать в клетки и использоваться для генерации аденозинтрифосфата
(вещество, которое имеет большое значение в обмене веществ и энергии в
организмах) в обход mTOR-пути в мозге. Рецептор и циклокреатин связаны
тем, что последний можно применять для питания в обход пути, который
подавляется сломанным рецептором", — пояснил один из авторов статьи,
руководитель группы по биоинформатике в лаборатории "Компьютерные
технологии" Университета ИТМО Алексей Сергушичев.
Исследователи из
Университета ИТМО в рамках этой научной работы создали вычислительный
метод, упрощающий интерпретацию экспериментальных данных для изучения
изменений в метаболизме клеток, который нарушается при сломанном TREM2.
Программа обнаруживает связи между изменениями в метаболизме и генах,
что позволяет ученым разобраться, как они функционируют.
https://ria.ru/science/2017...
Рейтинг публикации:
|